Wasserstoff Farbenlehre
| Grau | Blau | Grün |
| Etabliertes Verfahren zur Wasserstoffgewinnung. Sowohl die benötigte Energie als auch die Ausgangsstoffe stammen aus fossilen Stoffen wie Kohle oder Erdgas. Bei Temperaturen von 700 bis 1.000 °C und mit Hilfe von Wasserdampf wird aus einer Methanquelle Wasserstoff gewonnen und in weiteren Reaktionsschritten angereichert. Das Verfahren ist effizient und erprobt. Und leider klimaschädlich, denn jedes Kilogramm grauer Wasserstoff wird mit sieben Kilogramm CO2 „bezahlt“. 95 Prozent des heute produzierten Wasserstoffs sind grau. | Gewinnung von grauem Wasserstoff. Rohstoff sind also auch hier fossile Energieträger, aus denen Methandampf gewonnen und dann Wasserstoff abgeschieden wird. Das freiwerdende CO2 wird allerdings aufgefangen und entweder endgelagert (Injektion in unterirdische Sandsteinschichten) oder in der chemischen Industrie weiterverwendet. | Gewinnung von Wasserstoff durch Elektrolyse. Mit regenerativ erzeugter Energie wird Wasser in seine Bestandteile gespalten, Sauerstoff und Wasserstoff. Es wird kein CO2 freigesetzt. Allerdings ist die Energiebilanz noch verbesserungsfähig, weswegen bisher nur ein Bruchteil von Wasserstoff grün erzeugt wird. |
Die AEM-Elektrolyse
Bei der Produktion von grünem Wasserstoff wird regenerativ erzeugter Strom im Gleichstromformat verwendet. Dabei befinden sich die beiden Elektroden in einem Behälter, der sogenannten Zelle. Anode und Kathode sind durch eine teildurchlässige Membran getrennt. Eine Lauge oder Säure dient als Elektrolyt. Wird jetzt elektrischer Strom an die Elektroden (Kathode, negativer Pol und Anode, positiver Pol) angelegt, findet an beiden Elektroden eine chemische Reaktion statt. An der Kathode wird Wasserstoff freigesetzt, an der Anode spaltet sich Sauerstoff ab. Es entsteht ein einzelnes Wasserstoffatom und ein Restmolekül OH-. Das extrem reaktionsfreudige einzelne Wasserstoffatom verbindet sich sofort mit einem weiteren Wasserstoffatom und wird dann über eine Gasdiffusionsschicht abtransportiert und aufgefangen.
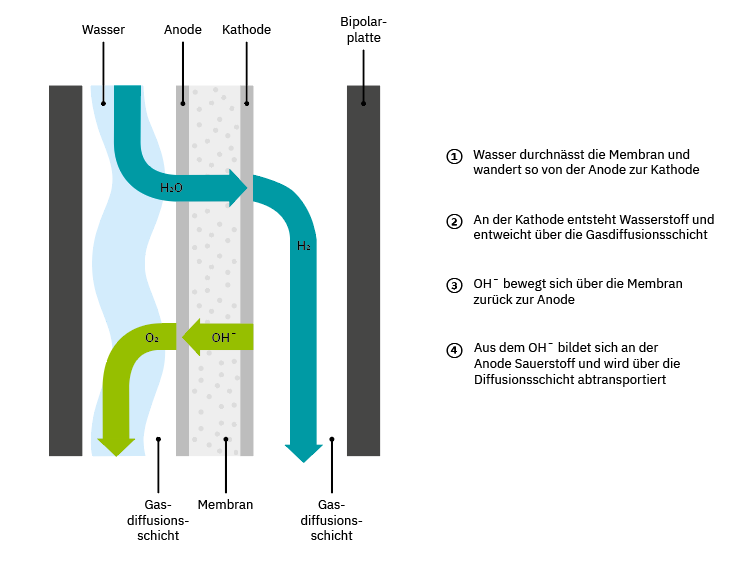
Die Zelle wird mit einer Membran geteilt, um die beiden Teile des gespaltenen Wassermoleküls zuverlässig getrennt zu halten. Kommen die nämlich zusammen, verbinden sie sich sofort wieder. Und das mit Schwung. Wenn diese Wiedervereinigung unkontrolliert abläuft, spricht man von einer Knallgasreaktion.






Bei dem von Enapter verwendeten Verfahren wird nur eine stark verdünnte Kaliumhydroxidlauge verwendet statt sonst üblicher starker Säuren. Die benötigen nämlich Platin und Titan für Behältnis und Elektroden, um der aggressiven Substanz langfristig widerstehen zu können. Beim AEM-Elektrolyseur reichen Stahl und nichtedle Metalle. Das macht den Elektrolyseur deutlich preiswerter und einfacher in der Handhabung. Durch eine ausgeklügelte Druckbeaufschlagung zwischen den Halbzellen erreicht Enapter einen hohen Reinheitsgrad des gewonnenen Wasserstoffs.



